1. Basiskennis (als je het experimentele deel wilt zien, ga dan direct naar het tweede deel)
Als een afgeleide reactie van conventionele PCR, bewaakt real-time PCR voornamelijk de verandering van de hoeveelheid amplificatieproduct in elke cyclus van de PCR-amplificatiereactie in realtime door de verandering van het fluorescentiesignaal, en analyseert kwantitatief het startsjabloon door de relatie tussen de ct-waarde en de standaardcurve.
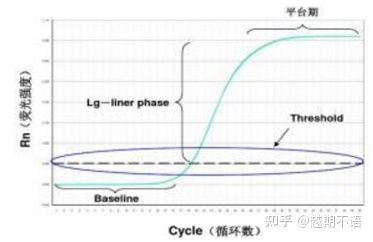
De specifieke gegevens van RT-PCR zijnbasislijn, fluorescentie drempelEnCt-waarde.
| basislijn: | De fluorescentiewaarde van de 3e-15e cyclus is de basislijn (baseline), die wordt veroorzaakt door de incidentele meetfout. |
| Drempel (drempel): | Verwijst naar de fluorescentiedetectielimiet die is ingesteld op een geschikte positie in het exponentiële groeigebied van de amplificatiecurve, doorgaans 10 keer de standaarddeviatie van de basislijn. |
| CT-waarde: | Het is het aantal PCR-cycli wanneer de fluorescentiewaarde in elke reageerbuis de drempel bereikt. De Ct-waarde is omgekeerd evenredig met de hoeveelheid initiële sjabloon. |
Gebruikelijke labelmethoden voor RT-PCR:
| methode | voordeel | Tekortkoming | toepassingsgebied |
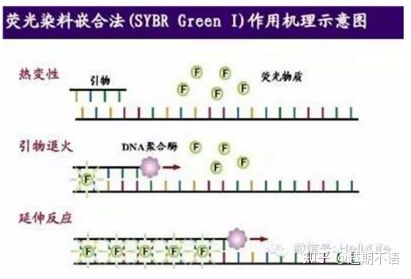
| SYBR GroenⅠ | Brede toepasbaarheid, gevoelig, goedkoop en handig | Primervereisten zijn hoog, vatbaar voor niet-specifieke banden | Het is geschikt voor kwantitatieve analyse van verschillende doelwitgenen, onderzoek naar genexpressie en onderzoek naar transgene recombinante dieren en planten. |
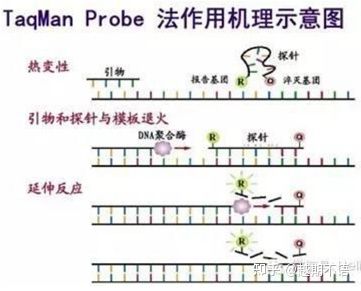
| TaqMan | Goede specificiteit en hoge herhaalbaarheid | De prijs is hoog en alleen geschikt voor specifieke doeleinden. | Detectie van ziekteverwekkers, genonderzoek naar geneesmiddelresistentie, beoordeling van de werkzaamheid van geneesmiddelen, diagnose van genetische ziekten. |
| moleculair baken | Hoge specificiteit, fluorescentie, lage achtergrond | De prijs is hoog, het is alleen geschikt voor een specifiek doel, het ontwerp is moeilijk en de prijs is hoog. | Specifieke genanalyse, SNP-analyse |
2. Experimentele stappen
2.1 Over de experimentele groepering- er moeten meerdere putten in de groep zijn en er moeten biologische herhalingen zijn.
| ① | Blanco controle | Wordt gebruikt om de celgroeistatus in experimenten te detecteren |
| ② | Negatieve controle siRNA (niet-specifieke siRNA-sequentie) | Demonstreer de specificiteit van RNAi-actie.siRNA kan een niet-specifieke stressrespons induceren bij een concentratie van 200 nM. |
| ③ | Transfectiereagenscontrole | Sluit de toxiciteit van het transfectiereagens voor de cellen of het effect op de expressie van het doelgen uit |
| ④ | siRNA tegen doelgen | Schakel de expressie van het doelgen uit |
| ⑤ (optioneel) | positief siRNA | Wordt gebruikt om experimentele systeem- en operationele problemen op te lossen |
| ⑥ (optioneel) | Fluorescerende controle siRNA | De efficiëntie van celtransfectie kan worden waargenomen met een microscoop |
2.2 Principes van primerontwerp
| Vergrote fragmentgrootte | Bij voorkeur op 100-150bp |
| Primer-lengte | 18-25 bp |
| GC-inhoud | 30%-70%, bij voorkeur 45%-55% |
| Tm-waarde | 58-60℃ |
| Reeks | Vermijd T/C continu;A/G continu |
| 3 einde reeks | Vermijd GC-rijk of AT-rijk;de terminalbasis is bij voorkeur G of C;het is het beste om T te vermijden |
| Complementariteit | Vermijd complementaire sequenties van meer dan 3 basen binnen de primer of tussen twee primers |
| Specificiteit | Gebruik explosiezoeken om de specificiteit van de primer te bevestigen |
①SiRNA is soortspecifiek en de sequenties van verschillende soorten zullen verschillend zijn.
②SiRNA is verpakt in gevriesdroogd poeder, dat bij kamertemperatuur 2-4 weken stabiel kan worden bewaard.
2.3 Hulpmiddelen of reagentia die vooraf moeten worden voorbereid
| Primer (interne referentie) | Inclusief vooruit en achteruit twee |
| Primers (doelgen) | Inclusief vooruit en achteruit twee |
| Doel Si RNA (3 strips) | Over het algemeen zal het bedrijf 3 strips synthetiseren en vervolgens een van de drie kiezen met RT-PCR |
| Transfectie Kit | Lipo2000 enz. |
| RNA snelle extractiekit | Voor RNA-extractie na transfectie |
| Snelle omgekeerde transcriptiekit | voor cDNA-synthese |
| PCR-amplificatiekit | 2×Super SYBR Groen qPCR-mastermix |
2.4 Met betrekking tot de kwesties waaraan aandacht moet worden besteed in de specifieke experimentele stappen:
① siRNA-transfectieproces
1. Voor plateren kunt u een plaat met 24 putjes, een plaat met 12 putjes of een plaat met 6 putjes kiezen (de gemiddelde RNA-concentratie die wordt voorgesteld in elk putje van een plaat met 24 putjes is ongeveer 100-300 ng/uL), en de optimale transfectiedichtheid van cellen is ongeveer 60%-80%
2. De transfectiestappen en specifieke vereisten zijn strikt in overeenstemming met de instructies.
3. Na transfectie kunnen monsters binnen 24-72 uur worden verzameld voor mRNA-detectie (RT-PCR) of eiwitdetectie binnen 48-96 uur (WB)
② RNA-extractieproces
1. Voorkom besmetting door exogene enzymen.Het omvat voornamelijk het strikt dragen van maskers en handschoenen;gebruik van gesteriliseerde pipetpunten en EP-buisjes;het water dat in het experiment wordt gebruikt, moet RNase-vrij zijn.
2. Het wordt aanbevolen om twee keer te doen zoals voorgesteld in de snelle extractiekit, wat de zuiverheid en opbrengst echt zal verbeteren.
3. De afvalvloeistof mag de RNA-kolom niet raken.
③ RNA-kwantificering
Nadat het RNA is geëxtraheerd, kan het direct worden gekwantificeerd met Nanodrop en de minimale aflezing kan zo laag zijn als 10ng/ul.
④Omgekeerd transcriptieproces
1. Vanwege de hoge gevoeligheid van RT-qPCR moeten voor elk monster ten minste 3 parallelle putjes worden gemaakt om te voorkomen dat de volgende Ct te verschillend is of dat de SD te groot is voor statistische analyse.
2. Master mix niet herhaaldelijk invriezen en ontdooien.
3. Elk buisje/gat moet worden vervangen door een nieuwe tip!Gebruik niet continu dezelfde pipetpunt om monsters toe te voegen!
4. De film die na het toevoegen van het monster aan de 96-wells-plaat is bevestigd, moet met een plaat worden gladgestreken.Het is het beste om te centrifugeren voordat je het op de machine zet, zodat de vloeistof op de buiswand naar beneden kan stromen en luchtbellen kan verwijderen.
⑤Gemeenschappelijke curve-analyse
| Geen periode van logaritmische groei | Mogelijk hoge concentratie van sjabloon |
| Geen CT-waarde | Onjuiste stappen voor het detecteren van fluorescentiesignalen; degradatie van primers of probes – de integriteit ervan kan worden gedetecteerd door PAGE-elektroforese; onvoldoende hoeveelheid sjabloon; degradatie van sjablonen - vermijden van de introductie van onzuiverheden en herhaaldelijk invriezen en ontdooien bij monstervoorbereiding; |
| Kt>38 | Lage versterkingsefficiëntie;PCR-product is te lang;verschillende reactiecomponenten worden afgebroken |
| Lineaire versterkingscurve | Sondes kunnen gedeeltelijk worden aangetast door herhaalde vries-dooicycli of langdurige blootstelling aan licht |
| Vooral het verschil in dubbele gaten is groot | De reactieoplossing is niet volledig gesmolten of de reactieoplossing is niet gemengd;het thermaalbad van het PCR-instrument is verontreinigd met fluorescerende stoffen |
2.5 Over data-analyse
De data-analyse van qPCR kan worden onderverdeeld in relatieve kwantificering en absolute kwantificering.Bijvoorbeeld cellen in de behandelingsgroep vergeleken met cellen in de controlegroep,
Hoe vaak het mRNA van het X-gen verandert, dit is relatieve kwantificering;in een bepaald aantal cellen het mRNA van het X-gen
Hoeveel exemplaren er zijn, dit is absolute kwantificering.Meestal gebruiken we in het laboratorium de relatieve kwantitatieve methode.Gebruikelijk,de 2-ΔΔct-methodewordt het meest gebruikt in experimenten, dus alleen deze methode zal hier in detail worden geïntroduceerd.
2-ΔΔct-methode: Het verkregen resultaat is het verschil in expressie van het doelwitgen in de experimentele groep ten opzichte van het doelwitgen in de controlegroep.Het is vereist dat de amplificatie-efficiëntie van zowel het doelgen als het interne referentiegen bijna 100% bedraagt en dat de relatieve afwijking niet groter is dan 5%.
De berekeningswijze is als volgt:
Δct-controlegroep = ct-waarde van doelgen in controlegroep – ct-waarde van intern referentiegen in controlegroep
Δct experimentele groep = ct-waarde van het doelgen in de experimentele groep – ct-waarde van het interne referentiegen in de experimentele groep
ΔΔct=Δct experimentele groep-Δct controlegroep
Bereken ten slotte het veelvoud van het verschil in uitdrukkingsniveau:
Wijzig Fold=2-ΔΔct (overeenkomend met de Excel-functie is POWER)
Gerelateerde producten:
Posttijd: 20 mei 2023