Op de Vaccine and Health Conference riepen experts op om "iedereen aandacht te schenken aan mRNA-vaccins, die de mens onbeperkt denken geven".Dus wat is precies een mRNA-vaccin?Hoe werd het ontdekt en wat is de toepassingswaarde ervan?Kan het de COVID-19 weerstaan die over de hele wereld raast?Heeft mijn land met succes een mRNA-vaccin ontwikkeld?Laten we vandaag eens kijken naar het heden en verleden van mRNA-vaccins.
01
Wat is mRNA in mRNA-vaccins?
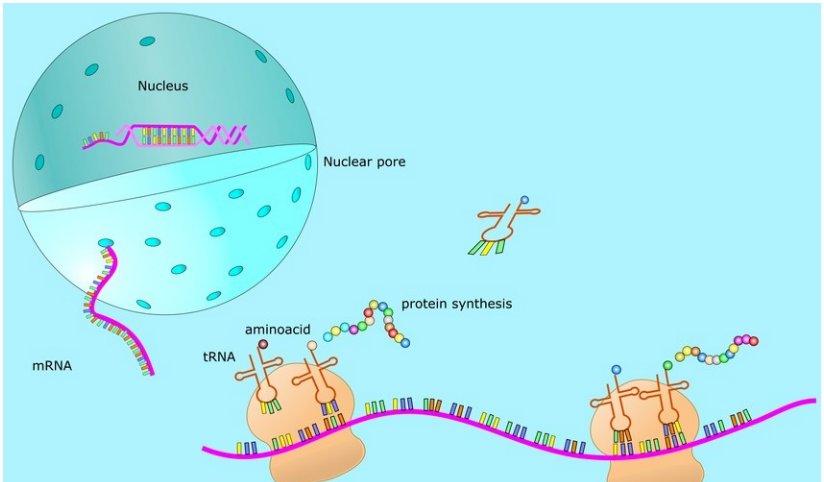
mRNA (Messenger RNA), dat wil zeggen boodschapper-RNA, is een type enkelstrengs RNA dat wordt getranscribeerd van een DNA-streng als een sjabloon en genetische informatie bevat die de eiwitsynthese kan sturen.In termen van de leek repliceert mRNA de genetische informatie van één streng dubbelstrengs DNA in de kern en verlaat vervolgens de kern om eiwitten in het cytoplasma te produceren.In het cytoplasma bewegen ribosomen langs het mRNA, lezen de basevolgorde en vertalen het naar het overeenkomstige aminozuur, en vormen uiteindelijk een eiwit (Figuur 1).
Figuur 1 mRNA werkproces
02
Wat is een mRNA-vaccin en wat maakt het uniek?
mRNA-vaccins introduceren mRNA dat codeert voor ziektespecifieke antigenen in het lichaam en gebruiken het eiwitsynthesemechanisme van de gastheercel om antigenen te genereren, waardoor een immuunrespons wordt geactiveerd.Gewoonlijk kunnen mRNA-sequenties van specifieke antigenen worden geconstrueerd volgens verschillende ziekten, verpakt en in cellen worden getransporteerd door nieuwe lipide nanocarrier-deeltjes, en vervolgens worden de mRNA-sequenties van menselijke ribosomen gebruikt om de mRNA-sequenties te vertalen om ziekte-antigeeneiwitten te produceren, die worden herkend door het auto-immuunsysteem na secretie om een immuunrespons te genereren, om de rol van ziektepreventie te bereiken (Figuur 2).
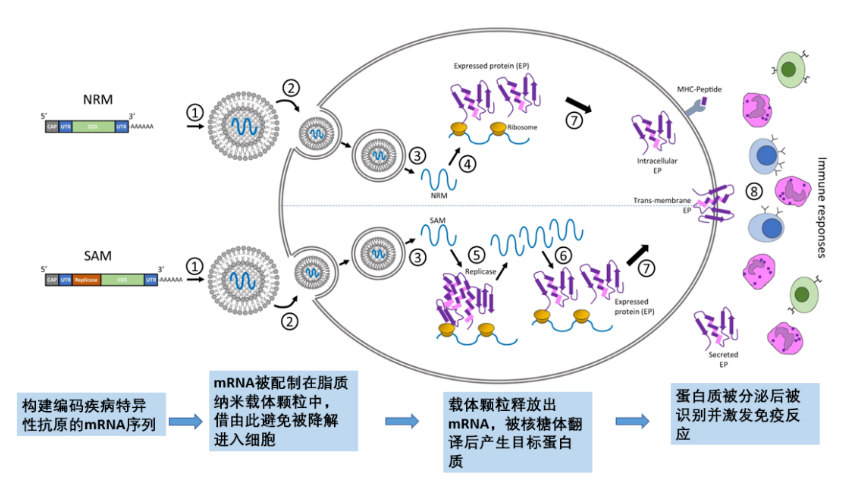 Figuur 2. In vivo effect van mRNA-vaccin
Figuur 2. In vivo effect van mRNA-vaccin
Wat is er dan uniek aan dit type mRNA-vaccin in vergelijking met traditionele vaccins?mRNA-vaccins zijn de meest geavanceerde vaccins van de derde generatie en verder onderzoek is nodig om hun stabiliteit te verbeteren, hun immunogeniciteit te reguleren en nieuwe toedieningstechnologieën te ontwikkelen.
De eerste generatie traditionele vaccins omvat voornamelijk geïnactiveerde vaccins en levende verzwakte vaccins, die het meest worden gebruikt.Geïnactiveerde vaccins verwijzen naar het eerst kweken van virussen of bacteriën en ze vervolgens inactiveren met hitte of chemicaliën (meestal formaline);levende verzwakte vaccins verwijzen naar ziekteverwekkers die na verschillende behandelingen muteren en hun toxiciteit verzwakken.maar behoudt nog steeds zijn immunogeniciteit.Het inoculeren ervan in het lichaam veroorzaakt geen ziekte, maar de ziekteverwekker kan groeien en zich vermenigvuldigen in het lichaam, de immuunrespons van het lichaam activeren en een rol spelen bij het verkrijgen van langdurige of levenslange bescherming.
De tweede generatie nieuwe vaccins omvat subeenheidvaccins en recombinant-eiwitvaccins.Subunit-vaccin is een vaccin-subunit-vaccin dat is gemaakt van de belangrijkste beschermende immunogene componenten van pathogene bacteriën, dat wil zeggen dat door chemische afbraak of gecontroleerde proteolyse de speciale eiwitstructuur van bacteriën en virussen wordt geëxtraheerd en uitgefilterd.Vaccins gemaakt van immunologisch actieve fragmenten;recombinant-eiwitvaccins zijn antigeen-recombinant-eiwitten die in verschillende celexpressiesystemen worden geproduceerd.
De derde generatie geavanceerde vaccins omvat DNA-vaccins en mRNA-vaccins.Het is om het virale genfragment (DNA of RNA) dat codeert voor een bepaald antigeen eiwit direct in de dierlijke somatische cellen te introduceren (vaccininjectie in het menselijk lichaam), en het antigene eiwit te produceren via het eiwitsynthesesysteem van de gastheercel, waardoor de gastheer om immuniteit te produceren tegen de antigene eiwitrespons om het doel van preventie en behandeling van ziekte te bereiken.Het verschil tussen de twee is dat DNA eerst wordt getranscribeerd in mRNA en vervolgens wordt eiwit gesynthetiseerd, terwijl mRNA direct wordt gesynthetiseerd.
03
De ontdekkingsgeschiedenis en toepassingswaarde van mRNA-vaccin
Als het gaat om mRNA-vaccins, moeten we een uitstekende vrouwelijke wetenschapper noemen, Kati Kariko, die een solide basis voor wetenschappelijk onderzoek heeft gelegd voor de komst van mRNA-vaccins.Ze was tijdens haar studie vol onderzoeksinteresse in mRNA.In haar meer dan 40-jarige wetenschappelijke onderzoekscarrière kreeg ze herhaaldelijk tegenslagen, vroeg ze geen fondsen voor wetenschappelijk onderzoek aan en had ze geen stabiele wetenschappelijke onderzoekspositie, maar ze heeft altijd aangedrongen op mRNA-onderzoek.
Er zijn drie belangrijke knooppunten in de komst van mRNA-vaccins.
In de eerste stap slaagde ze erin om via celkweek het gewenste mRNA-molecuul te produceren, maar ze stuitte op een probleem bij het laten functioneren van het mRNA in het lichaam: na het injecteren van het mRNA in de muis, zou het worden opgeslokt door het immuunsysteem van de muis.Toen ontmoette ze Weissman.Ze gebruikten een molecuul in tRNA genaamd pseudouridine om mRNA de immuunrespons te laten ontwijken.][2].
In de tweede stap, rond 2000, bestudeerde prof. Pieter Cullis lipide nanotechnologie LNP's voor in vivo afgifte van siRNA voor genuitschakelingstoepassingen [3][4].Weissman organisatie Kariko et al.ontdekte dat LNP in vivo een geschikte drager van mRNA is en een waardevol hulpmiddel kan worden voor het afleveren van mRNA dat codeert voor therapeutische eiwitten, en vervolgens geverifieerd bij de preventie van het zikavirus, hiv en tumoren [5] ][6][7][8].
In de derde stap, in 2010 en 2013, verkregen Moderna en BioNTech achtereenvolgens patentlicenties met betrekking tot mRNA-synthese van de Universiteit van Pennsylvania voor verdere ontwikkeling.Katalin werd in 2013 ook de senior vice-president van BioNTech om mRNA-vaccins verder te ontwikkelen.
Tegenwoordig kunnen mRNA-vaccins worden gebruikt bij infectieziekten, tumoren en astma.In het geval dat COVID-19 over de hele wereld raast, kunnen mRNA-vaccins een rol als voorhoede spelen.
04
Het toepassingsperspectief van mRNA-vaccin in COVID-19
Met de wereldwijde epidemie van COVID-19 werken landen hard aan de ontwikkeling van een vaccin om de epidemie te beteugelen.Als nieuw type vaccin heeft het mRNA-vaccin een leidende rol gespeeld bij de komst van de nieuwe kroonepidemie.Veel toptijdschriften hebben melding gemaakt van de rol van mRNA bij het nieuwe coronavirus SARS-CoV-2 (Figuur 3).
Figuur 3 Rapport over mRNA-vaccins ter voorkoming van nieuw coronavirus (van NCBI)
Allereerst hebben veel wetenschappers melding gemaakt van het onderzoek naar het mRNA-vaccin (SARS-CoV-2 mRNA) tegen het nieuwe coronavirus bij muizen.Bijvoorbeeld: een in lipidenanodeeltjes ingekapseld nucleoside-gemodificeerd mRNA (mRNA-LNP)-vaccin, een injectie met een enkele dosis induceert sterke type 1 CD4+ T- en CD8+ T-celresponsen, langlevende plasma- en geheugen-B-celresponsen en een robuuste en aanhoudende neutraliserende antilichaamrespons.Dit geeft aan dat het mRNA-LNP-vaccin een veelbelovende kandidaat is tegen COVID-19[9][10].
Ten tweede vergeleken sommige wetenschappers de effecten van SARS-CoV-2 mRNA en traditionele vaccins.Vergeleken met recombinante eiwitvaccins: mRNA-vaccins zijn verreweg superieur aan eiwitvaccins wat betreft kiemcentrumrespons, Tfh-activering, neutraliserende antilichaamproductie, specifieke geheugen-B-cellen en langlevende plasmacellen [11] .
Toen SARS-CoV-2 mRNA-vaccinkandidaten klinische proeven begonnen, ontstonden er zorgen over de korte duur van de vaccinbescherming.Wetenschappers hebben een in lipiden ingekapselde vorm van een nucleoside-gemodificeerd mRNA-vaccin ontwikkeld, mRNA-RBD genaamd.Een enkele injectie kan sterke neutraliserende antilichamen en cellulaire reacties genereren, en kan modelmuizen die zijn geïnfecteerd met 2019-nCoV bijna volledig beschermen, waarbij hoge niveaus van neutraliserende antilichamen gedurende ten minste 6,5 maand worden gehandhaafd.Deze gegevens suggereren dat een enkele dosis mRNA-RBD langdurige bescherming biedt tegen SARS-CoV-2-challenge [12].
Ook werken wetenschappers aan de ontwikkeling van nieuwe veilige en effectieve vaccins tegen COVID-19, zoals het BNT162b-vaccin.Beschermde makaken tegen SARS-CoV-2, beschermde de onderste luchtwegen tegen viraal RNA, produceerde zeer krachtige antilichamen en vertoonde geen tekenen van ziekteverergering.Twee kandidaten worden momenteel geëvalueerd in fase I-onderzoeken, en de evaluatie in wereldwijde fase II/III-onderzoeken is ook aan de gang, en de toepassing staat voor de deur [13].
05
De status van het mRNA-vaccin in de wereld
Op dit moment staan BioNTech, Moderna en CureVac bekend als 's werelds top drie leiders op het gebied van mRNA-therapie.Onder hen lopen BioNTech en Moderna voorop in het onderzoek naar en de ontwikkeling van het nieuwe kroonvaccin.Moderna richt zich op het onderzoek naar en de ontwikkeling van mRNA-gerelateerde medicijnen en vaccins.Het COVID-19 fase III-proefvaccin mRNA-1273 is het snelst groeiende project van het bedrijf.BioNTech is ook een wereldwijd toonaangevend bedrijf op het gebied van onderzoek en ontwikkeling van mRNA-geneesmiddelen en -vaccins, met in totaal 19 mRNA-geneesmiddelen/vaccins, waarvan er 7 de klinische fase zijn ingegaan.CureVac richt zich op het onderzoek naar en de ontwikkeling van mRNA-geneesmiddelen/vaccins en is het eerste bedrijf ter wereld dat een GMP-conforme RNA-productielijn opzet, gericht op tumoren, infectieziekten en zeldzame ziekten.
Gerelateerde producten:RNase-remmer
Sleutelwoorden: miRNA-vaccin, RNA-isolatie, RNA-extractie, RNase-remmer
Referenties:1.K Karikó, Buckstein M, Ni H, et al.Onderdrukking van RNA-herkenning door tolachtige receptoren: de impact van nucleosidemodificatie en de evolutionaire oorsprong van RNA [J].Immuniteit, 2005, 23(2):165-175.
2. K Karikó, Muramatsu H, Welsh FA, et al.Opname van Pseudouridine in mRNA levert superieure niet-immunogene vector op met verhoogde translationele capaciteit en biologische stabiliteit [J].Moleculaire therapie, 2008.3.Chonn A, Cullis PR.Recente ontwikkelingen in liposoomtechnologieën en hun toepassingen voor systemische genafgifte [J].Advanced Drug Delivery Reviews, 1998, 30(1-3):73.4.Kulkarni JA, Witzigmann D, Chen S, et al.Lipide-nanodeeltjestechnologie voor klinische vertaling van siRNA-therapieën[J].Rekeningen van chemisch onderzoek, 2019, 52(9).5.Kariko, Katalin, Madden, et al.Expressiekinetiek van nucleoside-gemodificeerd mRNA afgeleverd in lipide nanodeeltjes aan muizen via verschillende routes [J].Journal of Controlled Release Publicatieblad van de Controlled Release Society, 2015.6.Zika-virusbescherming door een enkele laaggedoseerde nucleoside-gemodificeerde mRNA-vaccinatie [J].Natuur, 2017, 543(7644):248-251.7.Pardi N, Secreto AJ, Shan X, et al.Toediening van nucleoside-gemodificeerd mRNA dat codeert voor een breed neutraliserend antilichaam beschermt gehumaniseerde muizen tegen hiv-1-challenge [J].Natuurcommunicatie, 2017, 8:14630.8.Stadler CR, B?Hr-Mahmud H, Celik L, et al.Eliminatie van grote tumoren bij muizen door mRNA-gecodeerde bispecifieke antilichamen [J].Natuurgeneeskunde, 2017.9.NN Zhang, Li XF, Deng YQ, et al.Een thermostabiel mRNA-vaccin tegen COVID-19[J].Cel, 2020.10.D Laczkó, Hogan MJ, Toulmin SA, et al.Een enkele immunisatie met nucleoside-gemodificeerde mRNA-vaccins lokt sterke cellulaire en humorale immuunresponsen uit tegen SARS-CoV-2 bij muizen - ScienceDirect[J].2020.11.Lederer K, Castao D, Atria DG, et al.SARS-CoV-2-mRNA-vaccins bevorderen krachtige antigeen-specifieke kiemcentrumreacties geassocieerd met neutraliserende antilichaamvorming [J].Immuniteit, 2020, 53(6):1281-1295.e5.12.Huang Q, Ji K, Tian S, et al.Een mRNA-vaccin met een enkele dosis biedt langdurige bescherming voor hACE2-transgene muizen tegen SARS-CoV-2[J].Natuurcommunicatie.13.Vogel AB, Kanevsky I, Ye C, et al.Immunogene BNT162b-vaccins beschermen resusapen tegen SARS-CoV-2[J].Natuur, 2021:1-10.
Posttijd: 20 juni 2022